阿姆斯特丹,2023年5月24日
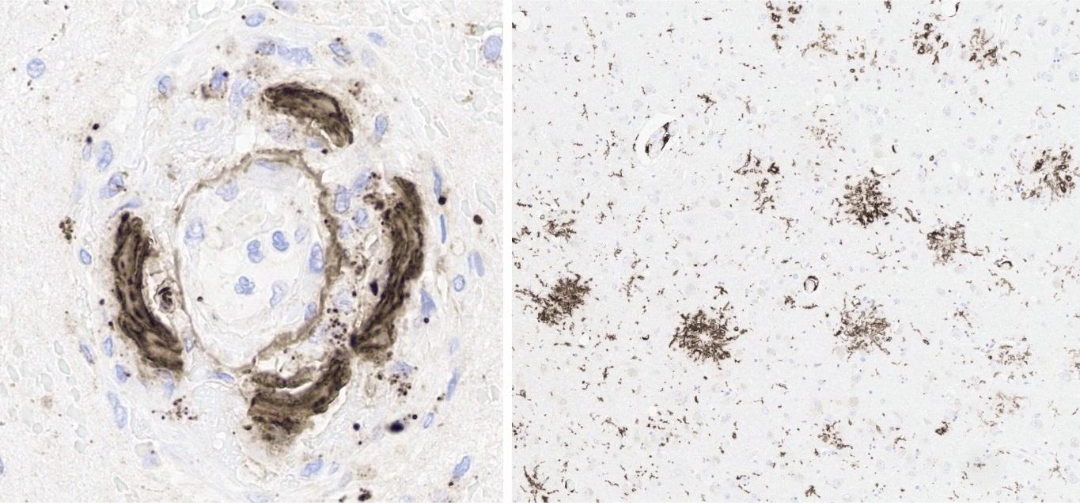
在一份发表于《阿尔茨海默病杂志》的引人注目的案例研究中,调查人员报告了一位患有阿尔茨海默病(AD)的65岁女性在接受实验性抗淀粉样蛋白β(Aβ)抗体药物Lecanemab的三次开放标签输注后的尸检结果。在最后一次输注后的四天,她出现了中风症状,并在数天后因多灶性颅内出血死亡,尽管进行了治疗干预。神经病理学结果显示,治疗诱导的Aβ吞噬作用涉及脑实质组织和脑血管中的纤维性Aβ。
关于AD发病机制的最广泛研究的理论是淀粉样蛋白级联假说,该假说认为Aβ过多以神经毒素的形式驱动AD的疾病过程,神经纤维退行、神经元丢失和神经功能恶化是下游事件。因此,减轻Aβ的存在将是一种合理的治疗干预策略。
该患者参与了一个关于实验性Lecanemab疗效和安全性的III期研究,Lecanemab是一种人源化单克隆治疗药物,被认为能够靶向可溶性Aβ原纤维。该试验显示,在18个月内,认知功能下降的速度减少了27%。先前的临床试验已经显示了针对Aβ的实验性治疗的不良反应的可能性。
首席研究员鲁道夫•J•卡斯特拉尼(Rudolph J. Castellani)博士解释说:“值得注意的是,尽管针对Aβ的临床试验已经进行了20多年,且已知有临床反应和影像学反应(与Aβ相关的影像学异常或ARIA),但我们基本上没有对这些实验性抗体的细胞反应或淀粉样清除机制有所了解,这个案例报告之前还没有这方面的见解。”卡斯特拉尼博士是美国伊利诺伊州芝加哥西北大学芬博格医学院病理学系的神经病理学教授。
在这个案例中,患者在接受Lecanemab仅三次输注后去世,处于对药物的“亚急性”反应阶段。这种发现在治疗方案的这一时刻之前尚未有报道。尽管尸检未发现明显的全身心血管并发症,但对大脑的检查确认了抗Aβ治疗导致了一种以往未描述的涉及脑皮质中无数小血管的淀粉样吞噬综合征,而这些小血管存在丰富的脑淀粉样血管病变(CAA)。这似乎导致了中风症状的发作,并在中风干预中引发了出血。
卡斯特拉尼博士评论道:“在这种情况下,我认为很明显,患者对抗Aβ治疗的反应导致了临床症状,并为出血干预提供了一个基质,这引发了潜在致命的药物相互作用的问题。那么问题就变成了,接受抗Aβ治疗的患者是否能够充分评估CAA的程度(在阿尔茨海默病中CAA的程度各不相同,从没有或很少CAA到丰富CAA,就像这个案例中一样),以及是否能够避免不良和潜在致命的结果。从积极的方面来看,Aβ和可能的磷酸化tau似乎部分被清除,后者以前从未被描述过。简而言之,取得了改善,但代价是小血管因CAA受损而受到间接伤害。”
共同研究员Pouya Jamshidi博士,芝加哥西北大学芬博格医学院病理学系警告说:“尽管这是首份详细描述对Lecanemab的神经病理学反应的报告案例,但病理学上的模式和分布是如此引人注目,以至于难以相信这将是个别事件。”
根据西北大学芬博格医学院神经病学系行为神经学首席教授、Mesulam认知神经学与阿尔茨海默病Mesulam中心的名字起源者M.-Marsel Mesulam博士的说法:“Lecanemab的问世为AD的治疗开启了新的阶段。从群体水平来看,益处并不明显,并且在个体患者中是不可预知的。副作用,即使很少出现症状,也可能具有毁灭性,正如这个病例报告所暗示的。对脑血管疾病和载脂蛋白E状态的筛查成为开药的重要环节。此外,可能需要告知患者,如果发生中风事件,抗凝治疗可能成为一个更高风险的选择。”
卡斯特拉尼博士补充说:“在Aβ靶向治疗和由CAA影响的血管之间,显然存在着微妙而危险的平衡。迫切需要更好的生物标志物来准确评估CAA的程度。神经影像学和APOE基因分型虽然对风险分层很重要,但无法检测出许多严重CAA的病例。”
《阿尔茨海默病杂志》的主编、德克萨斯大学圣安东尼奥分校Semmes杰出大学神经生物学讲座教授乔治•佩里(George Perry)博士指出:“这个案例的结果要求对那些因这些实验性药物而患病的人进行深入细致的审查,以最大程度地减少脑损伤和死亡的风险。”
编辑注意事项
该文章的标题是《抗淀粉样蛋白β免疫治疗的神经病理学:一份案例报告》,作者为Rudolph J. Castellani、Elisheva D. Shanes、Matthew McCord、Nicholas J. Reish、Margaret E. Flanagan、M-Marsel Mesulam和Pouya Jamshidi
文章翻译自:阿尔茨海默病杂志






评论 (0)