找到
53
篇与
AD知识
相关的结果
-
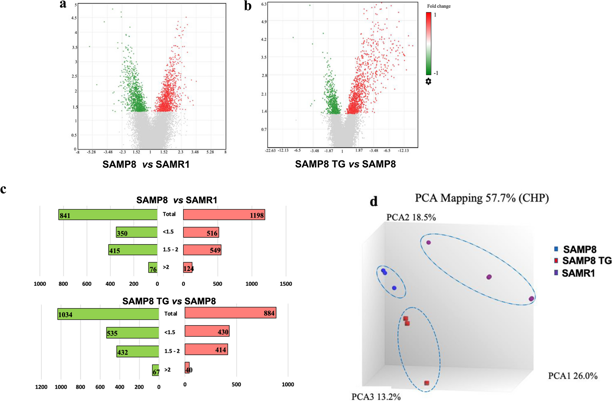
 科学家在咖啡中发现一种脑力促进剂 一项新的研究发现,咖啡和一些蔬菜中的天然化合物川芎嗪(TG)能显著增强老年小鼠的空间学习能力和记忆力。研究表明,TG 能改变关键的分子通路并减少神经炎症,这凸显了它在解决与年龄相关的认知能力下降方面的潜力。最近的研究越来越多地集中于寻找能够抵御与年龄相关的认知能力下降和促进健康老龄化的天然化合物。咖啡、葫芦巴种子和萝卜中含有的一种植物生物碱--三高碱(TG),被认为是增强认知能力的候选物质。在一项新的研究中,筑波大学的研究人员利用衰老加速小鼠易感基因 8(SAMP8)模型,从认知和分子生物学的角度综合研究了 TG 对记忆和空间学习(获取、保留、构建和应用与周围物理环境相关的信息)的影响。给 SAMP8 小鼠口服 TG 30 天后,与未服用 TG 的 SAMP8 小鼠相比,莫里斯水迷宫测试表明小鼠的空间学习和记忆能力有了显著提高。接下来,研究人员对海马进行了全基因组转录组分析,以探索潜在的分子机制。他们发现,与神经系统发育、线粒体功能、ATP合成、炎症、自噬和神经递质释放有关的信号通路在TG组中受到显著调节。此外,研究小组还发现,TG 通过负向调节信号因子 Traf6 介导的转录因子 NF-κB 激活,抑制了神经炎症。此外,蛋白质定量分析证实,炎症细胞因子 TNF-α 和 IL-6 的水平显著降低,海马中神经递质多巴胺、去甲肾上腺素和血清素的水平显著升高。这些研究结果表明,TG 能有效预防和改善与年龄相关的空间学习记忆损伤。这项工作得到了 DyDo DRINCO 和日本科学技术振兴机构(JST 基金编号 JPMJPF2017)的支持。文章来源:cnBeta.COM
科学家在咖啡中发现一种脑力促进剂 一项新的研究发现,咖啡和一些蔬菜中的天然化合物川芎嗪(TG)能显著增强老年小鼠的空间学习能力和记忆力。研究表明,TG 能改变关键的分子通路并减少神经炎症,这凸显了它在解决与年龄相关的认知能力下降方面的潜力。最近的研究越来越多地集中于寻找能够抵御与年龄相关的认知能力下降和促进健康老龄化的天然化合物。咖啡、葫芦巴种子和萝卜中含有的一种植物生物碱--三高碱(TG),被认为是增强认知能力的候选物质。在一项新的研究中,筑波大学的研究人员利用衰老加速小鼠易感基因 8(SAMP8)模型,从认知和分子生物学的角度综合研究了 TG 对记忆和空间学习(获取、保留、构建和应用与周围物理环境相关的信息)的影响。给 SAMP8 小鼠口服 TG 30 天后,与未服用 TG 的 SAMP8 小鼠相比,莫里斯水迷宫测试表明小鼠的空间学习和记忆能力有了显著提高。接下来,研究人员对海马进行了全基因组转录组分析,以探索潜在的分子机制。他们发现,与神经系统发育、线粒体功能、ATP合成、炎症、自噬和神经递质释放有关的信号通路在TG组中受到显著调节。此外,研究小组还发现,TG 通过负向调节信号因子 Traf6 介导的转录因子 NF-κB 激活,抑制了神经炎症。此外,蛋白质定量分析证实,炎症细胞因子 TNF-α 和 IL-6 的水平显著降低,海马中神经递质多巴胺、去甲肾上腺素和血清素的水平显著升高。这些研究结果表明,TG 能有效预防和改善与年龄相关的空间学习记忆损伤。这项工作得到了 DyDo DRINCO 和日本科学技术振兴机构(JST 基金编号 JPMJPF2017)的支持。文章来源:cnBeta.COM -
 阿尔茨海默氏症和痴呆症的 10 种早期体征和症状 扰乱日常生活的记忆力减退可能是阿尔茨海默氏症或其他痴呆症的症状。阿尔茨海默氏症是一种脑部疾病,会导致记忆力、思维和推理能力缓慢下降。有 10 个警告体征和症状。如果您注意到其中任何一个,请不要忽视它们。尽快安排与医生的预约。一、扰乱日常生活的记忆力减退阿尔茨海默病最常见的迹象之一,尤其是在早期阶段,是忘记最近学到的信息。其他包括忘记重要的日期或事件,一遍又一遍地问同样的问题,以及越来越需要依靠记忆辅助工具(例如,提醒笔记或电子设备)或家庭成员来处理他们过去自己处理的事情。典型的变化有时会忘记名字或约会,但后来会记住它们。二、规划或解决问题的挑战一些因阿尔茨海默氏症或其他痴呆而记忆发生变化的人可能会经历他们制定和遵循计划或处理数字的能力发生变化。他们可能难以遵循熟悉的食谱或跟踪每月账单。他们可能难以集中注意力,并且比以前需要更长的时间来做事。典型的变化在管理财务或家庭账单时偶尔会犯错误。三、难以完成熟悉的任务患有阿尔茨海默氏症或其他痴呆症记忆变化的人经常发现很难完成日常任务。有时,他们可能难以开车到熟悉的地点、整理购物清单或记住最喜欢的游戏规则。典型的变化偶尔需要帮助才能使用微波炉设置或录制电视节目。四、与时间或地点混淆患有阿尔茨海默氏症或其他痴呆症的人可能会忘记日期、季节和时间的流逝。如果某事没有立即发生,他们可能难以理解。有时他们可能会忘记自己在哪里或如何到达那里。典型的变化对星期几感到困惑,但稍后再弄清楚。五、难以理解视觉图像和空间关系一些患有阿尔茨海默氏症或其他痴呆症的人可能会出现视力变化。这可能会导致平衡困难或阅读困难。他们还可能在判断距离和确定颜色或对比度方面存在问题,从而导致驾驶问题。典型的变化与白内障有关的视力变化。六、口语或写作中单词的新问题患有阿尔茨海默氏症或其他痴呆症的人可能难以关注或加入对话。他们可能会在谈话中途停下来,不知道如何继续,或者他们可能会重复自己。他们可能在词汇方面遇到困难,难以命名熟悉的物体或使用错误的名称(例如,将“手表”称为“手钟”)。典型的变化有时很难找到正确的词。七、放错地方,失去回溯步骤的能力患有阿尔茨海默氏症或其他痴呆症的人可能会把东西放在不寻常的地方。他们可能会丢失东西,并且无法回头再次找到它们。他或她可能会指责他人偷窃,尤其是随着疾病的进展。典型的变化不时放错地方,并回溯步骤以找到它们。八、判断力下降或判断力差患有阿尔茨海默氏症或其他痴呆症的人可能会经历判断或决策的变化。例如,他们在处理金钱时可能会使用糟糕的判断力,或者不太注意梳理或保持自己的清洁。典型的变化偶尔做出错误的决定或错误,比如忘记更换车内机油。九、退出工作或社交活动患有阿尔茨海默氏症或其他痴呆症的人可能会经历保持或跟随对话的能力发生变化。因此,他们可能会退出爱好、社交活动或其他活动。他们可能难以跟上最喜欢的团队或活动。典型的变化有时对家庭或社会义务不感兴趣。十、情绪和性格的变化患有阿尔茨海默氏症或其他痴呆症的人可能会经历情绪和性格变化。他们可能会感到困惑、多疑、沮丧、恐惧或焦虑。他们可能很容易在家里、与朋友在一起或离开舒适区时感到不安。典型的变化发展非常具体的做事方式,当例行公事被打乱时变得烦躁。接受检查。早期发现很重要如果您发现自己或他人身上有一个或多个迹象,可能很难知道该怎么做。在与他人讨论这些变化时感到不确定或紧张是很自然的。表达对自己健康的担忧可能会使它们看起来更“真实”。或者,您可能害怕通过分享对他或她的能力或行为变化的观察而感到不安。然而,这些都是重大的健康问题,应该由医生进行评估,重要的是要采取行动弄清楚发生了什么。
阿尔茨海默氏症和痴呆症的 10 种早期体征和症状 扰乱日常生活的记忆力减退可能是阿尔茨海默氏症或其他痴呆症的症状。阿尔茨海默氏症是一种脑部疾病,会导致记忆力、思维和推理能力缓慢下降。有 10 个警告体征和症状。如果您注意到其中任何一个,请不要忽视它们。尽快安排与医生的预约。一、扰乱日常生活的记忆力减退阿尔茨海默病最常见的迹象之一,尤其是在早期阶段,是忘记最近学到的信息。其他包括忘记重要的日期或事件,一遍又一遍地问同样的问题,以及越来越需要依靠记忆辅助工具(例如,提醒笔记或电子设备)或家庭成员来处理他们过去自己处理的事情。典型的变化有时会忘记名字或约会,但后来会记住它们。二、规划或解决问题的挑战一些因阿尔茨海默氏症或其他痴呆而记忆发生变化的人可能会经历他们制定和遵循计划或处理数字的能力发生变化。他们可能难以遵循熟悉的食谱或跟踪每月账单。他们可能难以集中注意力,并且比以前需要更长的时间来做事。典型的变化在管理财务或家庭账单时偶尔会犯错误。三、难以完成熟悉的任务患有阿尔茨海默氏症或其他痴呆症记忆变化的人经常发现很难完成日常任务。有时,他们可能难以开车到熟悉的地点、整理购物清单或记住最喜欢的游戏规则。典型的变化偶尔需要帮助才能使用微波炉设置或录制电视节目。四、与时间或地点混淆患有阿尔茨海默氏症或其他痴呆症的人可能会忘记日期、季节和时间的流逝。如果某事没有立即发生,他们可能难以理解。有时他们可能会忘记自己在哪里或如何到达那里。典型的变化对星期几感到困惑,但稍后再弄清楚。五、难以理解视觉图像和空间关系一些患有阿尔茨海默氏症或其他痴呆症的人可能会出现视力变化。这可能会导致平衡困难或阅读困难。他们还可能在判断距离和确定颜色或对比度方面存在问题,从而导致驾驶问题。典型的变化与白内障有关的视力变化。六、口语或写作中单词的新问题患有阿尔茨海默氏症或其他痴呆症的人可能难以关注或加入对话。他们可能会在谈话中途停下来,不知道如何继续,或者他们可能会重复自己。他们可能在词汇方面遇到困难,难以命名熟悉的物体或使用错误的名称(例如,将“手表”称为“手钟”)。典型的变化有时很难找到正确的词。七、放错地方,失去回溯步骤的能力患有阿尔茨海默氏症或其他痴呆症的人可能会把东西放在不寻常的地方。他们可能会丢失东西,并且无法回头再次找到它们。他或她可能会指责他人偷窃,尤其是随着疾病的进展。典型的变化不时放错地方,并回溯步骤以找到它们。八、判断力下降或判断力差患有阿尔茨海默氏症或其他痴呆症的人可能会经历判断或决策的变化。例如,他们在处理金钱时可能会使用糟糕的判断力,或者不太注意梳理或保持自己的清洁。典型的变化偶尔做出错误的决定或错误,比如忘记更换车内机油。九、退出工作或社交活动患有阿尔茨海默氏症或其他痴呆症的人可能会经历保持或跟随对话的能力发生变化。因此,他们可能会退出爱好、社交活动或其他活动。他们可能难以跟上最喜欢的团队或活动。典型的变化有时对家庭或社会义务不感兴趣。十、情绪和性格的变化患有阿尔茨海默氏症或其他痴呆症的人可能会经历情绪和性格变化。他们可能会感到困惑、多疑、沮丧、恐惧或焦虑。他们可能很容易在家里、与朋友在一起或离开舒适区时感到不安。典型的变化发展非常具体的做事方式,当例行公事被打乱时变得烦躁。接受检查。早期发现很重要如果您发现自己或他人身上有一个或多个迹象,可能很难知道该怎么做。在与他人讨论这些变化时感到不确定或紧张是很自然的。表达对自己健康的担忧可能会使它们看起来更“真实”。或者,您可能害怕通过分享对他或她的能力或行为变化的观察而感到不安。然而,这些都是重大的健康问题,应该由医生进行评估,重要的是要采取行动弄清楚发生了什么。 -
 研究表明阿尔茨海默病患者大脑重要膳食抗氧化剂的水平低于正常水平 弗吉尼亚理工大学Carilion医学院的一名教员发表在《阿尔茨海默病杂志》上的一项新研究表明,阿尔茨海默病患者的大脑膳食叶黄素,玉米黄质,番茄红素和维生素E水平是正常大脑的一半。较高的叶黄素和玉米黄质膳食水平与更好的认知功能和降低患痴呆或阿尔茨海默病的风险密切相关。"这项研究首次证明了阿尔茨海默氏症大脑中重要膳食抗氧化剂的缺陷。这些结果与大型人群研究一致,这些研究发现,那些吃富含类胡萝卜素的饮食,或血液中叶黄素和玉米黄质含量高,或作为黄斑色素积累在视网膜中的人患阿尔茨海默病的风险显着降低",医学院基础科学教育系教授C. Kathleen Dorey说。"不仅如此,我们相信吃富含类胡萝卜素的饮食将有助于在所有年龄段保持大脑处于最佳状态。"类胡萝卜素与健康的大脑由于正常的大脑功能和对错误折叠蛋白质的反应不断产生反应性氧化分子,大脑容易受到累积氧化损伤的影响,这可以通过健康饮食提供的抗氧化剂来预防。类胡萝卜素是强大的抗氧化剂,常见于五颜六色的植物中。叶黄素在羽衣甘蓝和菠菜中含量特别丰富,玉米黄质在玉米和橙子辣椒中含量最高。北卡罗来纳州威尔逊市Craft Technologies的Dorey和Neal E. Craft 在2004年首次报道,大脑选择性地积累了类胡萝卜素,如叶黄素,玉米黄质和β-隐黄质。从那时起,世界各地的研究人员已经证明,黄斑色素中叶黄素和玉米黄质含量较高的人认知能力更好,饮食中叶黄素和玉米黄质含量最高或黄斑色素中积累的叶黄素和玉米黄质含量最高的人痴呆风险较低。拉什大学记忆与衰老项目跟踪了居住在芝加哥十多年的 1,000 多名参与者的饮食和认知表现,评估了他们的类胡萝卜素摄入量,发现那些遵循 MIND 饮食的人——食用更高水平的富含抗氧化剂的水果、坚果、蔬菜和鱼,以及较低水平的肉类和甜食——降低了阿尔茨海默病诊断的风险, 死前认知能力更高,阿尔茨海默病相关的脑病理学更少。此外,十年来总类胡萝卜素或叶黄素/玉米黄质摄入量最高的人患阿尔茨海默病的风险降低了50%。类胡萝卜素与大脑保护之间的相关性尽管研究强烈暗示类胡萝卜素可能保护大脑免受导致阿尔茨海默病的损害,但没有证据表明类胡萝卜素与该疾病相关。《阿尔茨海默病杂志》(Journal of Alzheimer's Disease)六月刊上的Dorey-Craft报告填补了这一空白。在一项对有和没有阿尔茨海默病脑病理学的大脑中类胡萝卜素的研究中,Dorey-Craft团队证明,患有阿尔茨海默病神经病理学的大脑的叶黄素,玉米黄质,番茄红素和生育酚的水平显着降低。番茄红素、玉米黄质和视黄醇的浓度是年龄匹配的大脑中没有阿尔茨海默病病理学的一半。诊断和限制未来的阿尔茨海默病阿尔茨海默病受试者大脑中选择性类胡萝卜素和生育酚缺乏的这一新证据进一步支持越来越多的证据表明,在阿尔茨海默病诊断之前和可能之后,更多的类胡萝卜素膳食摄入量可能会减缓认知能力下降。研究还表明,视网膜选择性地从饮食中积累叶黄素和玉米黄质,形成可见的黄色黄斑色素,增强视力并保护光感受器。通过无创测量患者的黄斑色素光密度,研究人员可以估计大脑中叶黄素和玉米黄质的浓度。“阿尔茨海默病新疗法的最新进展显示出令人兴奋的前景,作为减缓疾病进展的有效方法,” Dorey说 “如果我们的数据激励人们通过丰富多彩的饮食、丰富的类胡萝卜素和定期锻炼来保持大脑处于最佳状态,我会很高兴。现有的研究表明,这也可能降低痴呆的风险。"文章来源:Dorey CK,Gierhart D,Fitch KA,Crandell I,Craft NE.低叶黄素,视黄醇,番茄红素和生育酚在患有阿尔茨海默病的大脑的灰质和白质中。J 阿尔茨海默病杂志 2023;94(1):1-17。
研究表明阿尔茨海默病患者大脑重要膳食抗氧化剂的水平低于正常水平 弗吉尼亚理工大学Carilion医学院的一名教员发表在《阿尔茨海默病杂志》上的一项新研究表明,阿尔茨海默病患者的大脑膳食叶黄素,玉米黄质,番茄红素和维生素E水平是正常大脑的一半。较高的叶黄素和玉米黄质膳食水平与更好的认知功能和降低患痴呆或阿尔茨海默病的风险密切相关。"这项研究首次证明了阿尔茨海默氏症大脑中重要膳食抗氧化剂的缺陷。这些结果与大型人群研究一致,这些研究发现,那些吃富含类胡萝卜素的饮食,或血液中叶黄素和玉米黄质含量高,或作为黄斑色素积累在视网膜中的人患阿尔茨海默病的风险显着降低",医学院基础科学教育系教授C. Kathleen Dorey说。"不仅如此,我们相信吃富含类胡萝卜素的饮食将有助于在所有年龄段保持大脑处于最佳状态。"类胡萝卜素与健康的大脑由于正常的大脑功能和对错误折叠蛋白质的反应不断产生反应性氧化分子,大脑容易受到累积氧化损伤的影响,这可以通过健康饮食提供的抗氧化剂来预防。类胡萝卜素是强大的抗氧化剂,常见于五颜六色的植物中。叶黄素在羽衣甘蓝和菠菜中含量特别丰富,玉米黄质在玉米和橙子辣椒中含量最高。北卡罗来纳州威尔逊市Craft Technologies的Dorey和Neal E. Craft 在2004年首次报道,大脑选择性地积累了类胡萝卜素,如叶黄素,玉米黄质和β-隐黄质。从那时起,世界各地的研究人员已经证明,黄斑色素中叶黄素和玉米黄质含量较高的人认知能力更好,饮食中叶黄素和玉米黄质含量最高或黄斑色素中积累的叶黄素和玉米黄质含量最高的人痴呆风险较低。拉什大学记忆与衰老项目跟踪了居住在芝加哥十多年的 1,000 多名参与者的饮食和认知表现,评估了他们的类胡萝卜素摄入量,发现那些遵循 MIND 饮食的人——食用更高水平的富含抗氧化剂的水果、坚果、蔬菜和鱼,以及较低水平的肉类和甜食——降低了阿尔茨海默病诊断的风险, 死前认知能力更高,阿尔茨海默病相关的脑病理学更少。此外,十年来总类胡萝卜素或叶黄素/玉米黄质摄入量最高的人患阿尔茨海默病的风险降低了50%。类胡萝卜素与大脑保护之间的相关性尽管研究强烈暗示类胡萝卜素可能保护大脑免受导致阿尔茨海默病的损害,但没有证据表明类胡萝卜素与该疾病相关。《阿尔茨海默病杂志》(Journal of Alzheimer's Disease)六月刊上的Dorey-Craft报告填补了这一空白。在一项对有和没有阿尔茨海默病脑病理学的大脑中类胡萝卜素的研究中,Dorey-Craft团队证明,患有阿尔茨海默病神经病理学的大脑的叶黄素,玉米黄质,番茄红素和生育酚的水平显着降低。番茄红素、玉米黄质和视黄醇的浓度是年龄匹配的大脑中没有阿尔茨海默病病理学的一半。诊断和限制未来的阿尔茨海默病阿尔茨海默病受试者大脑中选择性类胡萝卜素和生育酚缺乏的这一新证据进一步支持越来越多的证据表明,在阿尔茨海默病诊断之前和可能之后,更多的类胡萝卜素膳食摄入量可能会减缓认知能力下降。研究还表明,视网膜选择性地从饮食中积累叶黄素和玉米黄质,形成可见的黄色黄斑色素,增强视力并保护光感受器。通过无创测量患者的黄斑色素光密度,研究人员可以估计大脑中叶黄素和玉米黄质的浓度。“阿尔茨海默病新疗法的最新进展显示出令人兴奋的前景,作为减缓疾病进展的有效方法,” Dorey说 “如果我们的数据激励人们通过丰富多彩的饮食、丰富的类胡萝卜素和定期锻炼来保持大脑处于最佳状态,我会很高兴。现有的研究表明,这也可能降低痴呆的风险。"文章来源:Dorey CK,Gierhart D,Fitch KA,Crandell I,Craft NE.低叶黄素,视黄醇,番茄红素和生育酚在患有阿尔茨海默病的大脑的灰质和白质中。J 阿尔茨海默病杂志 2023;94(1):1-17。 -
 新的早期阿尔茨海默氏症治疗显示认知改善 Heather Sandison博士的研究揭示了突破性的结果:多模式方法有望扭转认知能力下降的人口认知能力下降。美国加利福尼亚州恩西尼塔斯 - 阿尔茨海默病和相关痴呆症(ADRD)护理的领先专家Heather Sandison博士最近在《阿尔茨海默病杂志》上发表了一项开创性的研究,强调了认知能力下降个体认知功能的显着改善。该研究是第二项采用多模式,个性化护理计划的研究,并为管理和潜在逆转认知障碍提供了进一步的希望。这项研究,“认知能力下降人群的认知改善:多模式干预方法”,发表在阿尔茨海默病杂志卷(94)第(3)期,重点关注客观认知障碍(OCI)的个体,这是阿尔茨海默病的前兆。Sandison博士和她的团队从加利福尼亚州圣地亚哥地区招募了34名参与者,根据认知能力下降的潜在因素(例如生活方式改变,营养保健品支持和药物)接受全面干预。在六个月的时间里,参与者接受了定期的临床访问,并通过每周的电话获得持续的营养支持。使用剑桥脑科学(CBS)电池和蒙特利尔认知评估(MoCA)在基线,一个月,三个月和六个月时评估认知功能。研究结果非常令人鼓舞。经过六个月的干预,参与者表现出认知功能的显着改善。MoCA评分从19.6±3.1上升到21.7±6.2(p = 0.013),表明认知能力增强。此外,在CBS认知电池的所有领域都观察到显着改善,包括记忆,推理,语言能力和注意力。Sandison博士评论说:“看到患者改善并看到有意义的变化,不仅对患者而且对他们的亲人恢复认知功能,真是太有成就感了。我希望这些发现开始将轶事转化为统计数据的过程,更多的患者开始获得这种类型的治疗。这项研究的结果对阿尔茨海默氏症的研究和护理领域具有重要意义。目前,已有6万美国人被诊断出患有阿尔茨海默病,而且这个数字还在增长。这项研究强调了通过整体和个性化的方法解决认知能力下降的重要性,针对导致疾病进展的各种因素。该研究证明了多模式干预方法对认知障碍的可行性和影响。需要进一步的研究来验证和扩展这些发现。Sandison博士的研究代表了在理解和治疗与阿尔茨海默病相关的认知能力下降方面迈出的重要一步。它强调了对认知障碍患者进行个性化、全面护理的重要性,并为该领域的未来发展奠定了基础。关于Heather Sandison博士 Heather Sandison博士是一位着名的自然疗法医生,专门研究神经认知医学,也是Solcere和Marama的创始人。凭借在阿尔茨海默病和相关痴呆症(ADRD)护理方面的专业知识,Sandison博士致力于推进解决认知能力下降的综合方法。她的研究和临床工作重点是开发个性化的多模式干预措施,以改善认知障碍患者的认知功能和生活质量。她致力于推进阿尔茨海默氏症和认知能力下降管理的研究和创新方法,为患者和家庭提供希望。联系: 芭芭拉·泽贝希瑟·桑迪森博士 电话:805.648.1870参考文献:Sandison,Heather等人“在认知能力下降的人的个性化生活方式干预期间观察到认知改善。阿尔茨海默病杂志,2023 年,第 1-12 页,第 https://doi.org/10.3233/jad-230004 页。翻译自:阿尔茨海默病杂志
新的早期阿尔茨海默氏症治疗显示认知改善 Heather Sandison博士的研究揭示了突破性的结果:多模式方法有望扭转认知能力下降的人口认知能力下降。美国加利福尼亚州恩西尼塔斯 - 阿尔茨海默病和相关痴呆症(ADRD)护理的领先专家Heather Sandison博士最近在《阿尔茨海默病杂志》上发表了一项开创性的研究,强调了认知能力下降个体认知功能的显着改善。该研究是第二项采用多模式,个性化护理计划的研究,并为管理和潜在逆转认知障碍提供了进一步的希望。这项研究,“认知能力下降人群的认知改善:多模式干预方法”,发表在阿尔茨海默病杂志卷(94)第(3)期,重点关注客观认知障碍(OCI)的个体,这是阿尔茨海默病的前兆。Sandison博士和她的团队从加利福尼亚州圣地亚哥地区招募了34名参与者,根据认知能力下降的潜在因素(例如生活方式改变,营养保健品支持和药物)接受全面干预。在六个月的时间里,参与者接受了定期的临床访问,并通过每周的电话获得持续的营养支持。使用剑桥脑科学(CBS)电池和蒙特利尔认知评估(MoCA)在基线,一个月,三个月和六个月时评估认知功能。研究结果非常令人鼓舞。经过六个月的干预,参与者表现出认知功能的显着改善。MoCA评分从19.6±3.1上升到21.7±6.2(p = 0.013),表明认知能力增强。此外,在CBS认知电池的所有领域都观察到显着改善,包括记忆,推理,语言能力和注意力。Sandison博士评论说:“看到患者改善并看到有意义的变化,不仅对患者而且对他们的亲人恢复认知功能,真是太有成就感了。我希望这些发现开始将轶事转化为统计数据的过程,更多的患者开始获得这种类型的治疗。这项研究的结果对阿尔茨海默氏症的研究和护理领域具有重要意义。目前,已有6万美国人被诊断出患有阿尔茨海默病,而且这个数字还在增长。这项研究强调了通过整体和个性化的方法解决认知能力下降的重要性,针对导致疾病进展的各种因素。该研究证明了多模式干预方法对认知障碍的可行性和影响。需要进一步的研究来验证和扩展这些发现。Sandison博士的研究代表了在理解和治疗与阿尔茨海默病相关的认知能力下降方面迈出的重要一步。它强调了对认知障碍患者进行个性化、全面护理的重要性,并为该领域的未来发展奠定了基础。关于Heather Sandison博士 Heather Sandison博士是一位着名的自然疗法医生,专门研究神经认知医学,也是Solcere和Marama的创始人。凭借在阿尔茨海默病和相关痴呆症(ADRD)护理方面的专业知识,Sandison博士致力于推进解决认知能力下降的综合方法。她的研究和临床工作重点是开发个性化的多模式干预措施,以改善认知障碍患者的认知功能和生活质量。她致力于推进阿尔茨海默氏症和认知能力下降管理的研究和创新方法,为患者和家庭提供希望。联系: 芭芭拉·泽贝希瑟·桑迪森博士 电话:805.648.1870参考文献:Sandison,Heather等人“在认知能力下降的人的个性化生活方式干预期间观察到认知改善。阿尔茨海默病杂志,2023 年,第 1-12 页,第 https://doi.org/10.3233/jad-230004 页。翻译自:阿尔茨海默病杂志 -
 阿尔茨海默病的治疗靶点被发现 一项新研究发现抑制神经元的过度活跃机制,可以逆转与阿尔茨海默病相关的某些认知表现。《医学快讯》8月10日消息拉瓦尔大学(Laval University)和莱斯布里奇大学(University of Lethbridge)的科学家们成功地在阿尔茨海默病的动物模型中逆转了与阿尔茨海默病相关的某些认知表现。他们的研究结果发表在科学杂志《大脑》(Brain)上。研究于2023年8月8日发表在《Brain》(最新影响因子:14.5)杂志上“虽然这还没有在人类中得到证实,但我们相信我们发现的机制构成了一个非常有趣的治疗靶点,因为它不仅减缓了疾病的进展,而且部分恢复了某些认知功能,”该研究的领导者、医学院教授、拉瓦尔大学切尔沃脑研究中心(Cervo Brain Research Centre)的研究员 Yves De Koninck 评论说。之前的研究表明,即使在阿尔茨海默病症状出现之前,那些发展成这种疾病的人的脑活动就已经被打乱了。“大脑中存在神经元过度活跃和信号紊乱。我们的假设是,调节神经元活跃的机制,更具体地说,是负责抑制神经元信号的机制,被打乱了,”研究人员解释说。 “人脑中神经元信号的主要抑制剂是神经递质 γ-氨基丁酸(GABA)。它与协同转运蛋白钾离子-氯离子共转运体2(KCC2)密切合作。这是一个离子泵,位于细胞膜上,在神经元内外循环氯离子和钾离子,” De Koninck 教授说,“维持神经元细胞膜上的这种离子泵可以减缓或逆转这种病理。” 细胞膜上 KCC2 的缺失可导致神经元过度活跃。一项研究已经表明,已故阿尔茨海默病患者大脑中的 KCC2 水平降低。这给了我们研究 KCC2 在阿尔茨海默病动物模型中的作用的想法,”研究人员补充说。在小鼠实验中取得的有前景的结果为了做到这一点,科学家们使用了表达阿尔茨海默病表现的小鼠系。研究人员发现,当这些小鼠长到四个月大时,大脑中两个区域的 KCC2 水平下降:海马体和前额皮质。这两个区域受损也会影响到阿尔茨海默病患者。 根据这些结果,研究人员转向了他们实验室开发的一种分子——CLP290,这是一种 KCC2 激活剂,可以防止其耗竭。在短期内,给 KCC2 水平已经降低的小鼠施用这种分子改善了它们的空间记忆和社交行为。从长期来看,CLP290 保护了它们免受认知能力下降和神经元过度活跃的影响。 “我们的结果并不意味着 KCC2 的缺失会导致阿尔茨海默病,” De Koninck 教授坚持认为。“另一方面,它似乎确实会引起离子失衡,导致神经元过度活跃,从而导致神经元死亡。这表明,通过防止 KCC2 的缺失,我们可以减缓甚至逆转这种疾病的某些表现。”由于各种原因,CLP290 还不能直接用于人体。De Koninck 教授的团队正在寻找其他 KCC2 激活分子,使阿尔茨海默病患者能够很好地耐受。“我们已经开发出了新的分子,目前正在我们的实验室进行评估。在进行这项研究的同时,我们正在对用于人类阿尔茨海默病以外的其他用途的药物进行测试,以评估它们对 KCC2 的影响。重新定位现有的药物将加速这一新的治疗途径的工作,”研究人员强调。参考文献Source:Laval UniversityA therapeutic target for Alzheimer's disease discoveredReference:Iason Keramidis and others, Restoring neuronal chloride extrusion reverses cognitive decline linked to Alzheimer’s disease mutations, Brain, 2023;, awad250, https://doi.org/10.1093/brain/awad250文章摘录于:阿尔茨海默病
阿尔茨海默病的治疗靶点被发现 一项新研究发现抑制神经元的过度活跃机制,可以逆转与阿尔茨海默病相关的某些认知表现。《医学快讯》8月10日消息拉瓦尔大学(Laval University)和莱斯布里奇大学(University of Lethbridge)的科学家们成功地在阿尔茨海默病的动物模型中逆转了与阿尔茨海默病相关的某些认知表现。他们的研究结果发表在科学杂志《大脑》(Brain)上。研究于2023年8月8日发表在《Brain》(最新影响因子:14.5)杂志上“虽然这还没有在人类中得到证实,但我们相信我们发现的机制构成了一个非常有趣的治疗靶点,因为它不仅减缓了疾病的进展,而且部分恢复了某些认知功能,”该研究的领导者、医学院教授、拉瓦尔大学切尔沃脑研究中心(Cervo Brain Research Centre)的研究员 Yves De Koninck 评论说。之前的研究表明,即使在阿尔茨海默病症状出现之前,那些发展成这种疾病的人的脑活动就已经被打乱了。“大脑中存在神经元过度活跃和信号紊乱。我们的假设是,调节神经元活跃的机制,更具体地说,是负责抑制神经元信号的机制,被打乱了,”研究人员解释说。 “人脑中神经元信号的主要抑制剂是神经递质 γ-氨基丁酸(GABA)。它与协同转运蛋白钾离子-氯离子共转运体2(KCC2)密切合作。这是一个离子泵,位于细胞膜上,在神经元内外循环氯离子和钾离子,” De Koninck 教授说,“维持神经元细胞膜上的这种离子泵可以减缓或逆转这种病理。” 细胞膜上 KCC2 的缺失可导致神经元过度活跃。一项研究已经表明,已故阿尔茨海默病患者大脑中的 KCC2 水平降低。这给了我们研究 KCC2 在阿尔茨海默病动物模型中的作用的想法,”研究人员补充说。在小鼠实验中取得的有前景的结果为了做到这一点,科学家们使用了表达阿尔茨海默病表现的小鼠系。研究人员发现,当这些小鼠长到四个月大时,大脑中两个区域的 KCC2 水平下降:海马体和前额皮质。这两个区域受损也会影响到阿尔茨海默病患者。 根据这些结果,研究人员转向了他们实验室开发的一种分子——CLP290,这是一种 KCC2 激活剂,可以防止其耗竭。在短期内,给 KCC2 水平已经降低的小鼠施用这种分子改善了它们的空间记忆和社交行为。从长期来看,CLP290 保护了它们免受认知能力下降和神经元过度活跃的影响。 “我们的结果并不意味着 KCC2 的缺失会导致阿尔茨海默病,” De Koninck 教授坚持认为。“另一方面,它似乎确实会引起离子失衡,导致神经元过度活跃,从而导致神经元死亡。这表明,通过防止 KCC2 的缺失,我们可以减缓甚至逆转这种疾病的某些表现。”由于各种原因,CLP290 还不能直接用于人体。De Koninck 教授的团队正在寻找其他 KCC2 激活分子,使阿尔茨海默病患者能够很好地耐受。“我们已经开发出了新的分子,目前正在我们的实验室进行评估。在进行这项研究的同时,我们正在对用于人类阿尔茨海默病以外的其他用途的药物进行测试,以评估它们对 KCC2 的影响。重新定位现有的药物将加速这一新的治疗途径的工作,”研究人员强调。参考文献Source:Laval UniversityA therapeutic target for Alzheimer's disease discoveredReference:Iason Keramidis and others, Restoring neuronal chloride extrusion reverses cognitive decline linked to Alzheimer’s disease mutations, Brain, 2023;, awad250, https://doi.org/10.1093/brain/awad250文章摘录于:阿尔茨海默病